鸡传染性贫血 (chicken infectious anemia,CIA)是由鸡传染性贫血病毒(chicken infectious anemia virus,CIAV)引起的一种免疫抑制性传染病。该病的主要特征为再生障碍性贫血和全身淋巴组织萎缩 [1] 。感染该病后鸡群对其他病原易感性增加,对疫苗免疫后的应答能力下降,给养鸡业造成严重的经济损失 [2] 。各日龄和品种鸡均可感染发病,2~3 周龄鸡多发,随着鸡日龄的增加,对该病的感染性下降,肉鸡比蛋鸡多发,公鸡发病率高于母鸡。1979 年,日本学者 Yuasa 报道了该病,随后英国、瑞典、加拿大等国均有相关报道 [3] ,我国亦于 1992 年分离到 CIAV [4] 。CIAV 是圆环病毒科环病毒属,病毒粒子大小约 23~25nm,球形,无囊膜,对外界环境抵抗力较强,鸡场一旦感染,难以清除。CIAV 不能凝集红细胞,为单股负链环状 DNA,基因组大小约为 2.3kb,包括 3 个开放阅读框(ORF)、ORF1、ORF2、ORF3 分别编码 VP1、VP2、VP3 蛋白。其中VP1 为病毒的衣壳蛋白,VP2 是辅助蛋白,帮助 VP1 装配成衣壳,VP3 又被称作凋亡素,是 CAV 诱导细胞凋亡的主要蛋白。该病的潜伏期为 8~12 天,一般在感染后的 10 天发病,病鸡和带毒鸡是传染源,病鸡胸腺和肝脏中含毒量最高。该病既能水平传播也能垂直传播,水平传播主要通过消化道和呼吸道传播,病毒通过鸡的分泌物和排泄物污染饲料、饮水及周围环境,引起其他鸡感染,水平传播一般不引起鸡发病,只产生抗体反应 [5] 。成鸡感染后不发病,但可通过种蛋垂直传递病原,蛋种鸡感染病毒后 3~6 周后的蛋带毒量较高。雏鸡体内有母源抗体时不发病,但可向环境排毒,公鸡也能通过精子传播该病毒。当与其他疾病混合感染时,病情加重,早期诊断对该病的防控具有重要的意义。可根据疾病的流行病学、临床症状和病理变化对该病做出初步诊断,要想确诊必须进行实验室诊断,因此有必要建立一种快速、灵敏的CIAV 实验室诊断方法。
CIAV 实验室诊断方法主要包括病毒分离鉴定 [6] 、血清中和试验、间接免疫荧光试验 [7] 、酶联免疫吸附试验(ELISA)、常规 PCR 方法 [8] 、环介导等温扩增技术 [9] 和荧光定量 PCR 检测方法等,这些方法在敏感性、特异性和时效性等方面都存在各自的不足,尤其不适于 CIAV 感染的早期快速诊断。比如病毒分离鉴定操作繁琐、耗时长,血清学方法敏感性低,不能早期检测;常规 PCR 技术不能对病毒定量,环介导等温扩增技术易出现假阳性结果等缺点。荧光定量 PCR技术经过 20 多年发展已经成熟,SYBR GreenⅠ染料法与 TaqMan 探针法相比,特异性太差,不适合临床检测,笔者以为荧光 PCR 探针法检测是当前较适合临床应用检测的技术,现已到了大规模推广应用荧光 PCR 检测病料样品的最佳时期。本文建立了 CIAV 荧光 PCR 检测方法,为 CIA 的早期快速诊断、流行病学调查、防控和净化工作奠定了基础。
1、材料和方法
1.1 病毒与病料
CIAV、禽呼肠孤病毒(ARV)、马立克氏病病毒(MDV)、禽白血病病毒(ALV)、禽网状内皮组织增生病病毒 (REV) 和传染性法氏囊病病毒(IBDV)由本实验室保存。临床检测病料为采自山东省各地鸡场临床诊断为 CIAV 感染的鸡肝脏、胸腺和脾脏等。
1.2 试剂和试剂盒
M-MLV 反转录酶、RNasin、dNTPs、DL2000Marker 等为宝生物工程(大连)有限公司产品,2×RealStar Probe Fast Mixture 为北京康润生物科技有限公司产品 ,AxyPrep 体液病毒DNA/RNA 小量试剂盒为爱思进生物技术(杭州)有限公司产品。
1.3 引物和探针
根据 GenBank 中收录的 CIAV 基因组序列(登录号:AF311892),应用生物学软件分别设计1 对引物及 TaqMan 探针,其中 1 对引物及相应的探针扩增 CIAV 疫苗毒株,引物序列为 CIAV-F1:5′- GATCAACCCAAGCCTCCCT -3′和CIAV-R1:5′- CCATCTTACAGTCTTATACAC-CTTC -3′,特异性探针为 P1:5′- FAM- CGATCCTGCGACCCCTCCGAGT-BHQ1-3′,
1.4 病毒核酸的提取
按 AxyPrep 体液病毒 DNA/RNA 小量试剂盒使用说明书提取 CIAV、ARV、MDV、ALV、REV 和 IBDV 等核酸作为模板。
1.5 荧光 PCR 检测方法的建立和优化
体系总体积为 25μL:2×RealStar ProbeFast Mixture 12.5μL,CIAV-F1、CIAV-R1 和 P1各若干,模板 1μL,其余用 RNase free dH2O 补齐。离心数秒后,放入 MyGo mini 荧光定量 PCR仪实时荧光定量 PCR 仪进行实时 PCR 扩增,对荧光 PCR 的程序进行优化,同时对反应体系中的引物和探针浓度进行筛选,以获得最低的CT 值和较高的荧光强度增加值。
1.6 荧光 PCR 的灵敏度
参照文献 [10] 测定 CIAV TCID 50 。将病毒培养液进行 10 倍系列稀释,取 100μL 病毒稀释液,经 AxyPrep 体液病毒 DNA/RNA 小量试剂盒抽提核酸后,进行荧光 PCR 检测,重复 3 次,确定最低的检测灵敏度。
1.7 荧光 PCR 的特异性、重复性试验
利用建立起的荧光 PCR 法分别对 CIAV、ARV、MDV、ALV、REV 和 IBDV 进行检测,验证其特异性。对 CIAV 的细胞培养液分别 10 倍系列稀释,每个梯度同时重复检测 3 次后,记录CT 值,然后分别计算对 CIAV 组内检测的变异系数。
1.8 临床样品检测
用建立的双重荧光定量 PCR 法对从山东省各地收集的临床疑似病料 63 份进行 CIAV检测,同时用常规 PCR 法进行检测,并比较二者检测结果。
2、结果
2.1 荧光 RT-PCR 反应条件的优化
优化结果表明,在 25 μL 反应体系中,扩增效果较好的引物和探针浓度分别为 :1μL CIAV-F1 (10μmol/L),1.2μL CIAV-R1(10μmol/L),0.8μL P1(5μmol/L),优化后的反应程序如下 :95℃ 预变性 5min,95℃ 变性10s,55℃退火 10s,72℃延伸 10s (此处收集荧光)。
2.2 荧光 PCR 的灵敏度
CIAV 细胞培养液病毒滴度为 10 3.43TCID 50 /100μL。当病毒株等比稀释到10 -3 ,即病毒滴度稀释到 2.69 TCID 50 /100μL 时,荧光 PCR扩增结果仍为阳性。
2.3 特异性检验
按建立方法对 CIAV、ARV、MDV、ALV、REV 和 IBDV 的阳性样品进行荧光定量 PCR检测,CIAV 样品孔 FAM 荧光检测出现了单一的 S 型扩增曲线,检测结果说明鸡传染性贫血疫苗毒株阳性。其余样品孔 FAM 荧光检测均没有 S 型扩增曲线,表明建立的荧光 PCR 检测方法特异性良好。
2.4 荧光 PCR 重复性试验
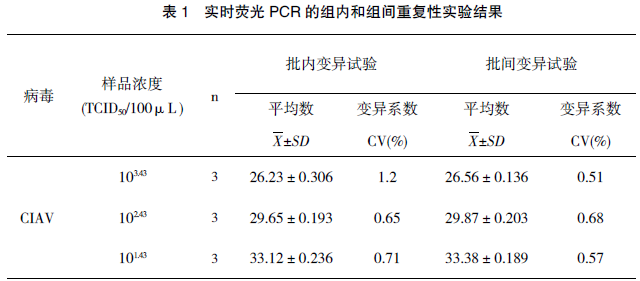
对 CIAV 细胞培养液 10 倍系列稀释,每个梯度同时重复检测 3 次后,利用建立起的荧光PCR 法进行检测,记录 CT 值,然后分别计算CIAV 组内、组间检测的变异系数,结果样品的Ct 值批内重复性试验 CV 值均小于 2.0%,批间重复性试验 CV 值均小于 1.0%,表明本方法的重复性好(表 1)。
2.5 临床样品检测
分别用建立荧光定量 PCR 和普通 PCR 方法,对临床收集的 63 份疑似 CIAV 感染样品进行检测,并与常规 PCR 检测方法进行比较。荧光定量 PCR 结果显示 63 份病料中有 8 份为CIAV 阳性,阳性率为 12.7%。常规 PCR 结果显示 63 份病料中有 6 份为阳性,检出率为 9.5%;荧光定量 PCR 检出率高于普通 PCR。
3、讨论
郭翠丽等 [11] 建立了一种快速检测 CIAV 的TaqMan 实时荧光定量 PCR 方法,同时验证其特异性、灵敏性和重复性。结果显示该法灵敏度可达 1.8×101 拷贝 /μL,远高于常规 PCR 方法;并与其他禽类病毒无交叉反应,具有高特异性。杨丽聪等 [12] 建立了 CIAV 的 SYBR GreenⅠ实时荧光定量 PCR 检测方法,并进行敏感性试验、特异性试验和重复性试验。结果显示,CIAV 的Ct 阈值与标准品浓度在 5.33×108 至 5.33×103拷贝 /μL 间呈良好的线性关系,相关系数R2=0.998,斜率为 -3.443,产物 Tm 值在 86℃左右。该方法与 REV、ALV-J 亚型、MDV、IBDV 基因组均无交叉反应,敏感性为 5.33 拷贝 /μL,比普通 PCR 高 1 000 倍,批内和批间重复试验变异系数均小于 3%。
核酸提取是 PCR 检测的重要步骤,核酸提取的时间和质量对 PCR 检测的总时间和检测的效果均有重要的影响。本研究采用商品化核酸试剂提取核酸,其主要采用吸附柱式,操作简单、快速,提取时配合小型高速离心机,能同时提取 DNA 和 RNA ,半小时即能完成提取过程。笔者将经典的 SDS- 蛋白酶 K 法与该法进行比对,结果检测结果一致,说明提取的 DNA质量完全能满足检测要求,重要的是该法核酸提取的时间远少于传统的 SDS- 蛋白酶 K 法法。与磁珠相比的优势是所需要的试剂少,操作简单,试剂常温保存即可,贮存和运输不需要低温,适合现场检测。
本研究采用 CIAV 一步法荧光 PCR 检测方法,可在 55min 完成扩增反应,得出检测结果,不需特定实验室,无需电泳,至少可节省 1/2 的时间和费用。该法操作简单,避免了由于多次操作及电泳而造成的污染问题,可检测微量病毒,将人为因素对结果的影响降到最低。试验所用的荧光定量 PCR 仪尺寸小,重量轻,便于携带,适合用于现场快速检测,从而节省送样的时间和样品运送途中的损耗,进一步提高检测的准确性,进而提早采取相应的防控措施,减少养殖场的经济损失。为了更加满足现场检测的需求,笔者下一步将对检测试剂的保存方式进行优化,将所用检测试剂配制完成后,加入冻干保护剂,并分装到 8 联管中冻干保存,常温保存和运输即可,使用时,只需要加入灭菌纯化水和模板,即能进行扩增反应。这样简化加样步骤,避免操作过程的污染。
本实验建立了 CIAV 一步法双重荧光 PCR检测方法,可用于现场检测 CIAV,特异性好,灵敏度高,稳定性好,配合 AxyPrep 体液病毒DNA/RNA 小量试剂盒,从核酸提取到报告检测结果仅需 1.5h,检测速度快,操作简便,适合现场检测。下一步可开发组装成试剂盒,市场前景很好,适合基层临床鸡传染性贫血的快速诊断,从而制定相应的防治措施,使损失降到最低,也可用于种鸡场所用活疫苗中 CIAV 外源病毒的快速检测,避免因种鸡场接种疫苗感染 CIAV的风险,同时也为 CIA 的流行病学调查及 CIA防控净化工作创造了有利的条件。
参考文献
[1] 李锋,黄炳亮.鸡传染性贫血病的研究进展及其展望[J].莱阳农学院学报,1992,(01):64-69.
[2] 张国中,赵继勋.鸡传染性贫血病的流行病学与诊断[J].兽医导刊,2009,(04):19-20+28.
[3] 殷震,刘景华.动物病毒学(第 2 版)[M].北京:科学出版社,1997:1175-1180.
[4] 崔现兰,幸桂香,吴东来,等.鸡传染性贫血病病毒的鉴定[J].中国畜禽传染病,1992,(06):3-5.
[5] 熊永忠,王秀荣,王笑梅.鸡传染性贫血病流行特点与诊断方法[J].黑龙江畜牧兽医,2002,(09):27-28.
[6] 林欢,么帅,脱添蓓,等.一株鸡传染性贫血病毒的分离鉴定及全基因组序列分析[J].中国预防兽医学报,2017,39(06):435-438.
[7] 王秀荣,王笑梅,李建伟,等.利用间接免疫荧光技术检测鸡传染性贫血病毒抗体[J].中国兽医科技,1998,(08):24-25.
[8] 杨兵,徐福洲,王金洛,等.应用 PCR 方法检测鸡传染性贫血病毒 [J]. 华北农学报,2003,(03):90-92.
[9] 邓显文,谢芝勋,谢志勤,等.鸡传染性贫血病毒病 LAMP 快速可视化检测方法的建立 [J].家畜生态学报,2011,32(06):57-60.
[10] 李延鹏,崔治中.一株 CIAV 野毒株致病性及其全基因组序列比较[J].微生物学报,2007,(05):894-898.
[11] 郭翠丽,张春红,郭鹏举,等.鸡传染性贫血病病毒 TaqMan 实时荧光定量 PCR 检测方法的建立[J].中国畜牧兽医,2014,41(12):45-49.
[12] 杨丽聪,苏霞,朱瑞豪,等.鸡传染性贫血病毒 SYBR Green Ⅰ实时荧光定量 PCR 检测方法的建立 [J]. 中 国 畜 牧 兽 医 ,2015,42 (04):859-864.
作者:于新友1,李天芝2(1.山东绿都生物科技有限公司,山东滨州256600 2.山东省滨州畜牧兽医研究院,山东滨州256600)
基金项目:山东省现代农业产业技术体系家禽创新团队项目(SDAIT-11-16)
作者简介:于新友(1983-),男,山东菏泽人,执业兽医师,硕士,主要从事动物传染病诊断及防控研究.
责任编辑:曹伟胜







