近几年来,鸡大肠杆菌流行及发病情况日趋严重,成年鸡以慢性感染或亚急性感染为主,雏鸡多呈败血症经过。如果有应激因素或混有其他病原体感染则病情更为复杂。目前,鸡的大肠杆菌病主要表现肠炎型、气囊炎型、卵黄性腹膜炎和肉芽肿型等,造成产蛋鸡大量减产、雏鸡死亡或发育迟缓。在成年鸡和青年鸡,还往往与新城疫、禽流感、传染性支气管炎、支原体和传染性鼻炎等混合感染,给防御和治疗带来困难。同时大肠杆菌多重耐药和交叉耐药日趋严重。大肠杆菌对药物的应变能力和适应环境的能力比较强,随着抗菌药物广泛、长期的使用,大肠杆菌的耐药性越来越严重,给临床治疗带来了困难。在治疗上如果不进行药敏试验已经难以筛选出高效的治疗药物。因此,准确地调查大肠杆菌对抗菌药物的敏感性是临床微生物实验室的一项主要工作之一。本实验研究从滨州市 3 个县分离到 10 株大肠杆菌,对此进行了分离培养、生化鉴定和药敏试验。
1、材料与方法
1.1 样品的采取及培养
用无菌棉拭子蘸取鸡直肠黏液,采样后接种于麦康凯培养基平板,将平板放置于 37℃恒温培养箱培养 20 h,然后无菌操作挑取单个典型的菌落接种于普通琼脂平板上分区划线进行纯培养,37℃恒温培养箱培养 20 h,培养结束后将平板放置于 4℃冰箱中备用。
1.2 细菌分离培养特性
将分离纯培养的大肠杆菌分别接种于麦康凯和伊红美蓝培养基,37℃培养 20 h,观察菌落特征。
由表 1 可知,分离出来的细菌培养特性符合大肠杆菌的菌落特征。

1.3 细菌的形态学观察
用接种环挑取生理盐水在洁净的载玻片上,然后挑取半个菌落与玻片上的水混匀,均匀涂抹开成蚕豆大的菌膜,自然干燥,在火焰上方来回中速固定 3 次,以玻片背面不烫手为准。进行革兰染色,步骤是:草酸铵结晶紫染液染色 1 min 水洗,卢戈氏碘染液染色 1 min 水洗,95%乙醇 30 s 到 1 min 脱色水洗,稀释复红染色 30 s 水洗,注意乙醇脱色到没有紫色脱下为止。吸水纸吸干,显微镜油镜下观察待检细菌的形态。
显微镜镜检可见革兰阴性杆菌,直短杆状,多数有鞭毛,能运动,部分菌株有菌毛(图 1)。
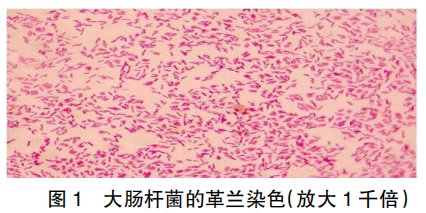
1.4 生化实验鉴定结果
由表 2 结果显示,大肠杆菌对乳糖、蔗糖、葡萄糖、三糖铁、吲哚和 MR 为阳性,对 VP、H2S结果为阴性,符合大肠杆菌的生化特征。

综合细菌的形态学观察、细菌的培养特性表明菌株为大肠杆菌,生化鉴定的结果进一步证明了菌株为大肠杆菌 [1] 。
1.5 肉汤中生长现象
分离出来的纯种菌株接种于肉汤中,放置于 37℃恒温培养箱培养,20 h 后肉汤呈现均匀混浊、液面管壁出现菌环,试管底部有黏性沉淀。
1.6 血清型鉴定
血清型鉴定按照中国兽医药品监察所提供的产品使用说明书进行操作,分别为 O1 、O2 、O24和 O7 。然后通过试管凝集反应试验鉴定。定型标准是血清试管凝集价大于等于 1∶640。
1.7 致病性实验
分离的菌株接种于 20 只雏鸡,有 12 只鸡在注射后 16~48 h 全部死亡,4 只鸡在 8 d 内死亡,剩下的 4 只鸡呈现一过性发病,48~72 h后逐渐饮水和采食。对死亡的鸡进行剖检,呈败血症经过,内脏有不同程度的出血、水肿,气囊表面有干酪样黄色渗出物,有的表现心包炎、肝周炎和心包积液。 采取死亡的鸡标本,均分离培养出了大肠杆菌。而且死亡越早的鸡,菌落在伊红 – 美蓝培养基上光泽越强。耐过的鸡进行解剖,发现心脏、肝、脾、肾有充血,盲肠和十二指肠出血。
1.8 药敏试验
敏感是指分离菌株能被测试药物使用推荐量时在感染部位通常可达到的抗菌药物浓度所抑制。而耐药性是指所分离的菌株不被测试药物常规剂量可达到的药物浓度所抑制或证明分离菌株可能存在某些特定的耐药机制,或治疗研究显示药物对分离菌株的临床疗效不可靠 [2] 。
药敏试验采用的是纸片扩散法(K-B 法)。该法操作简单,成本低廉,选药灵活,被 WHO推荐为定性药敏试验的基本方法,是目前应用较广泛的药敏试验方法。
1.8.1 配制 0.5 麦氏比浊度的菌液
用无菌棉拭子蘸取麦康凯培养基上的 3 个典型菌落,在无菌试管中用无菌生理盐水稀释,用细菌比浊仪测量细菌的浓度,校正菌液浓度至 0.5 麦氏比浊度,0.5 麦氏比浊度相当于1.5×108 /mL 的含菌量。
1.8.2 接种
用无菌棉拭子蘸取配制好的菌液,在管内壁将多余菌液旋转挤去后,在琼脂表面均匀涂抹接种 3 次,每次旋转 60°,最后沿平板内缘涂抹 1 周,目的是使细菌均匀涂布在平板上 [3] 。
1.8.3 贴放药敏纸片
将琼脂平板放置室温 3 min,用无菌镊子将药纸片紧贴于琼脂表面,用镊尖轻轻压一下纸片,使纸片紧贴在平板上。贴纸片时纸片距离平板边缘 >15 mm,各纸片中心距离 >24 mm,注意药敏片一旦与平板接触,不能再移动,因为药敏纸片与培养基接触后,纸片上药物已经开始扩散到培养基中了 [4] 。
1.8.4 培养
将贴好药敏片的培养基放置在 37℃恒温培养箱中培养 20h,要求每个平板单独平放,不能叠放,目的是让平板受热均匀。
1.8.5 结果判定
贴有药敏片的培养基在 37℃恒温培养箱培养 18h 后取出,用直尺测量抑菌圈的直径,抑菌圈的边缘应是无明显细菌生长的区域。根据CLSI 标准,对抑菌圈直径作出“敏感”、 “耐药”、“中度”的判断。药敏结果判定标准:>20 mm 为高度敏感,10~20 mm 为中度敏感,<10 mm 为低度敏感。
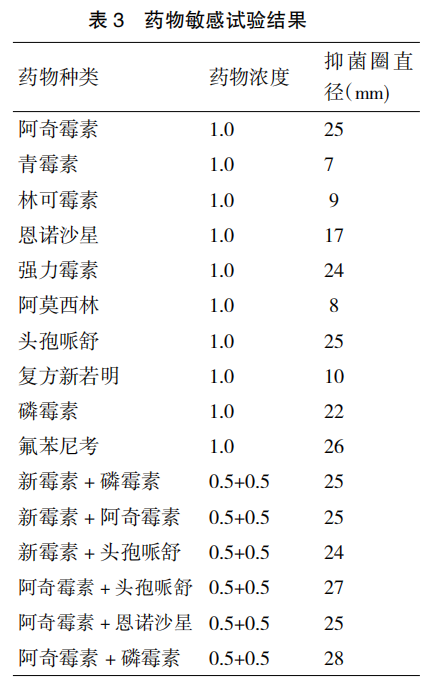
药物敏感实验结果显示(表 3),鸡大肠杆菌分离株耐药性严重,对青霉素、林可霉素、阿莫西林和复方新若明等已经产生耐药性。对阿奇霉素、强力霉素、头孢哌舒、磷霉素和氟苯尼考等大肠杆菌较为敏感。新霉素与磷霉素、阿奇霉素和头孢哌舒之间的药物组合,效果更好,并且降低了药物的费用。这对临床应用提供了参考,但是药物残留问题和耐药性的问题不断出现,还必须探索研究新的有效方法来预防和治疗鸡的大肠杆菌病。
2、分析讨论
根据对滨州市周围 3 个县养鸡集中区的调查,发现在规模养殖场疾病中大肠杆菌病占了首位,并且大肠杆菌血清型多,耐药菌株不断增加。本研究通过对发病鸡群大肠杆菌分离培养、形态学观察、生化鉴定、致病性实验和药敏试验,为明确滨州地区大肠杆菌的流行病学提供了依据,同时为滨州地区鸡大肠杆菌病的药物防治积累了经验,对养鸡场健康发展有重要的指导意义。
参考文献
[1] 李守远. 济南地区鸡大肠杆菌的分离鉴定及自家灭活疫苗研制[D]. 山东农业大学硕士论文,2013 ,23(10):171-174.
[2] 孟志敏,李连缺.河北省鸡源大肠杆菌分离鉴定及耐药性分析[J].养禽与禽病防治, 2010,10(05)145-146.
[3] 高华,张琼,严世平.347 株粪肠球菌耐药性分析[J].中华医院感染学杂志, 2011, 23(12):172-174.
作者:宋红娟(山东省滨州职业学院医疗学院,山东滨州256603)
责任编辑:曹伟胜







