沙门氏菌(Salmonella)是可感染人类和家畜、禽类等动物的革兰氏阴性肠道杆菌,家禽、肉类产品等是沙门氏菌致病的主要传播媒介 [1-3] 。在全球范围内,沙门氏菌感染是处于首要地位的食源性致病菌。沙门氏菌是重要的人畜共患病的病原体,可引起食物中毒、伤寒、败血症和慢性肠炎等疾病 [4-5] 。免疫力较弱人群(如婴幼儿、免疫缺陷个体等)感染沙门氏菌后通常病症较为严重,甚至导致死亡。羽绒是目前四大天然保暖材料(此外包括棉花、羊毛和蚕丝)中保暖性能较佳的材料之一 [6] 。随着人们消费水平的提高,消费者对羽绒制品的需求和质量要求的提升,羽绒羽毛原料及其制品的质量问题受到消费者的广泛关注。羽绒羽毛一般是鹅鸭等家禽制品,若在制成服装、枕头、被子等前处理不当或后期污染,可能检出有害微生物 [7-8] 。目前国家标准对羽绒羽毛及其制品的沙门氏菌要求是不得检出/20g [11] 。能力验证是利用实验室间比对,按照预先制定的准则评价参加者的能力;能力验证是重要的外部质量评价活动 [9-10] 。本实验室通过参加中国检科院测试评价中心组织的 A-CAS-PT211(2016)羽绒羽毛微生物检测能力验证来核查实验室检测人员的检测技术水平,对实验室整体检测流程进行评价,验证试验所用的仪器设备、试剂耗材和培养基等,识别检测过程中可能存在的问题并及时实施改进措施。
1、材料与方法
1.1 待测样品
ACAS-PT211(2016)羽绒羽毛微生物检测能力验证,锡箔纸密封袋真空包装,冷藏运输到实验室, 共 2 袋,样品编码为 16-D012 和16-L230,由中国检验检疫科学研究院测试评价中心提供。
1.2 主要培养基及试剂
蛋白胨、TTB 肉汤、亮绿琼脂、DHL 琼脂、革兰氏染液、三糖铁琼脂、尿素琼脂均为北京陆桥技术有限公司产品;赖氨酸脱羧酶等生化试剂为广东环凯微生物科技有限公司产品;氯化钠为国药集团化学试剂有限公司产品;A-F 多价 O 血清为兰州生物制品研究所产品;VITEK2GN 鉴定卡,为法国生物梅里埃公司产品;科马嘉沙门氏菌显色琼脂购自法国科马嘉产品;沙门氏菌标准菌株鼠伤寒沙门氏菌 ATCC14028,为美国菌种保藏中心产品。
1.3 主要仪器
BSC-1300ⅡA2 生物安全柜,苏净安泰空气技术有限公司;生化培养箱,上海一恒科技有限公司;滤器,广东环凯微生物科技有限公司;高压灭菌锅,美国致微(厦门)仪器有限公司;VITEK2 Compact 全自动微生物鉴定系统,法国生物梅里埃公司。
1.4 方法
按照《ACAS-PT211(2016)羽绒羽毛微生物检测能力验证参试指导书》 和《GB/T10288-2003 羽绒羽毛检测方法》[12]的要求进行样品前处理、增菌、分离和鉴定。同时采用生化试剂盒和全自动微生物鉴定系统(VITEK2-Compact)进行菌种鉴定 [13-14] ,最终结合以上实验结果出具原始记录,上报检测结果。检测流程图见图 1。同时以鼠伤寒沙门氏菌(ATCC14028)作为阳性对照试验。
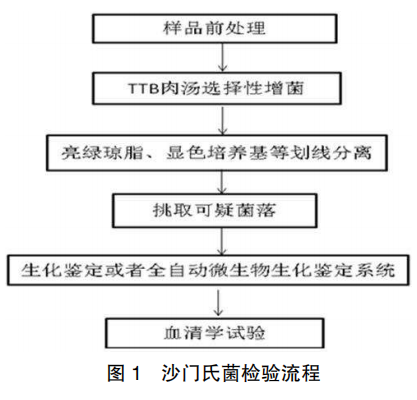
1.4.1 样品前处理
无菌操作开启样品,立即加入 1 200 mL0.1%的蛋白胨生理盐水,封上样品袋自封口,左右振荡混匀 3 min,切勿颠倒混匀;混匀后样品直接通过无菌纱布过滤。滤液作为样品原液进行检测。
1.4.2 增菌与分离
将上述 1 000 mL 滤液在滤器上过滤,滤膜取下无菌接种于 100 mL TTB 肉汤中,(43±2℃)水浴培养 15~18 h。培养后分别从增菌肉汤中接种一环于亮绿琼脂、DHL 琼脂和科马嘉沙氏琼脂显色琼脂培养基上进行划线分离,置37℃培养 24 h 后观察有无典型或者可疑沙门氏菌属的菌落。
1.4.3 鉴定
从各选择性琼脂平板上分别挑取典型或者可疑菌落,分别接种三糖铁培养基、尿素琼脂,同时接种营养琼脂 37℃上培养 24 h 后进行生化鉴定(赖氨酸脱羧酶、氰化钾、靛基质、甘露醇、山梨醇、ONPG)和应用全自动微生物鉴定系统(VITEK2-Compact)进行沙门氏菌生化鉴定,同时进行革兰氏染色。
将生化试验结果符合沙门氏菌属特性的菌株接种营养琼脂上,37℃纯培养 24 h 后用沙门氏菌 A-F 多价 O 血清进行鉴定,同时用生理盐水作对照。
2、结果与分析
2.1 分离培养
分离菌落形态描述见表 1。
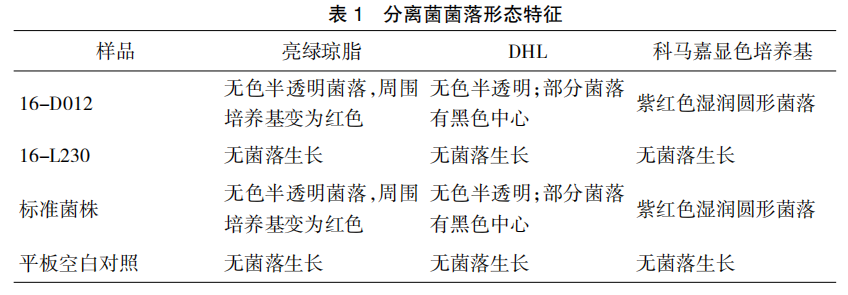
2.2 生化试验
上述 16-D012 样品的各平板上的菌落形态均为沙门 氏 菌的 典型 菌落,初 步判 断16-D012 为可疑菌落,将不同平板上分离得到的可疑菌落接种到营养琼脂进行纯培养,用于进一步的生化鉴定或者血清学试验。详细生化结果见表 2。利用 16-D012样品可疑菌落的纯培养物进行VITEK2 Compact 生化系统鉴定,鉴定结果为沙门氏菌群,98%置信度。
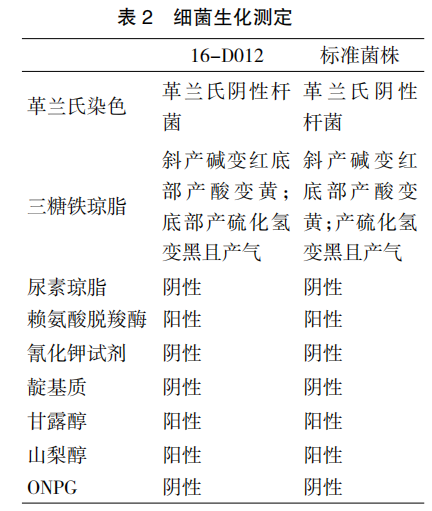
2.3 血清学试验
取可疑菌落和阳性对照的纯培养物、无菌生理盐水溶液(阴性对照),用沙门氏菌 A-F 多价诊断血清做玻片凝集试验。16-D012 菌株 A-F 多价 O 血清凝集。
3、结论
本次能力验证主要依据 GB/T10288-2003和 ACAS-PT211(2016)参试指导书对样品进行前处理、增菌培养、划线分离、镜检和生化鉴定等步骤检测,最终确定沙门氏菌项目的检测结果:16-D012 为检出 /10g,16-L230 为未检出/10g,且后期中国检验检疫科学研究院测试评价中心给出的能力验证结果评价为满意。本次能力验证参考多个检测标准,使用多种培养基和生化鉴定手段来确定最终检测结果。如使用科马嘉显色平板选择性较强,避免其他干扰菌对实验结果的干扰,方便实验室检测人员对沙门氏菌疑似菌落的辨识,最后结合 3 种平板综合分析,增加检测结果的准确性。在生化鉴定过程中采用了生化试剂盒与生化鉴定系统相结合的判定手段,确保检测结果的可靠性。在实际检测工作中,样品往往存在多种干扰菌,与目标菌菌落形态或生化相近,实验室条件允许情况下,可以选择不同选择性平板进行筛选分离后,结合生化试验来分析判断。血清鉴定试验中,沙门氏菌属目前已知的有 2 500 多种血清型 [16] ,市面上在售的沙门氏菌血清价格比较高且保存周期较短,本次能力验证过程只进行了简单的 A-F多价血清的鉴定,实验室条件允许的,可以结合生化作进一步的血清学分型鉴定。
参考文献
[1] Raghunathan A,Reed J,Shin S,et a1.Con-straint-based analysis of metabolic capacity of Salmonella typhimuriumduring host-pathogen in-teraction[J].BMC Systems Biology,2009,3(9):38.
[2]曾艳兵,张莉,孙吉昌,等.利用荧光定量 PCR检测方法对畜禽肉中沙门氏菌的污染调查[J].农产品质量与安全.2012:22-24.
[3] 刘卫兵. 上海地区和其他来源沙门氏菌多样性及其分子基础[D].上海交通大学.2011:1-10.
[4]Currie A, MacDougall L, Aramini J, et al. Frozen chicken nuggets and strips and eggs are leading risk factors for Salmonella Heidelberg infections in Canada[J]. Epidemiol Infect, 2005, 133(5): 809-816.
[5]饶振华,王宏,张苏,等.饲料中沙门氏菌的检测及其在肉骨粉中的生长特性研究[J].农产品质量与安全,2013,4:41-43.
[6]张克和,陈宇,俞旭霞,等.鹅鸭羽毛羽绒结构特征分析[J].中国纤检,2011(5) : 45-47.
[7]管政;陈爱亮.毛干 DNA 提取方法概述[J].中国生物工程杂志;2012,32(10):128-134.
[8]郑淑芬,李小红,梁淑茹.浅谈羽绒制品填充料质量问题[J].中国纤检,2015(1) : 60-61.
[9]中国合格评定国家认可委员会.CNAS-RL02:2016 能力验证规则[S].北京:中国标准出版社,2016:3.
[10]毛燕,闫林.实验室参加能力验证活动的意义分析 [J]. 食品安全质量检测学报.2014.9(5):2958-2961.
[11]马冲先.能力验证及其评价[J].理化检验 – 化学分册.2005.41:861-870.
[12] 中华人民共和国国家质量监督检验检疫总局. GB/T 10288-2003 羽绒羽毛检验方法 [S]. 北京:中国标准出版社,2003.
[13]中华人民共和国卫生部.GB 4789.4-2010 食品安全国家标准 食品微生物学检验 沙门氏菌检验[S].北京:中国标准出版社,2010.
[14] 中华人民共和国国家卫生和计划生育委员会.GB 4789.4-2016 食品安全国家标准 食品微生物学检验 沙门氏菌检验[S].北京:中国标准出版社,2016.
[15]王丽玲.能力验证、实验室间比对常用统计技术及评定方法[J].中国卫生检验杂志.2006.16(8):985-986.
[16]Bopp C A,Brenner FW,Fields P I,et a1.Es-cheriehia,ShigeUa and Sallmonella in manual of clinical microbiology[M].Washington DC:American Society for Microbiology Press,2003:654-671.
作者:吴卫玲1,2 ,钟君杰 1,2 ,胡同静 1,3 , 葛晴颖 1,3 , 朱振华 1 ,鞠慧萍 1,3(1 江苏省苏州出入境检验检疫局,江苏苏州 215104;2 江苏省苏州世标检测技术有限公司,江苏苏州 215104:3 江苏省苏州华博日化品检测服务有限公司,江苏苏州 215104)
作者简介:吴卫玲(1987-),女,汉,工程师,硕士研究生,纺织品化妆品微生物学。E-mail: 18251184276@163.com。电话:18251184276
责任编辑:李斐







