为切实做好 2018 年动物疫病强制免疫工作,农业部组织制订了“2018 年国家动物疫病强制免疫计划”,对高致病性禽流感的免疫动物种类和区域明确要求为:对全国所有鸡、水禽(鸭、鹅)、人工饲养的鹌鹑和鸽子等,进行 H5 亚型和 H7 亚型高致病性禽流感免疫。供研究和疫苗生产用的家禽、进口国(地区)明确要求不得实施高致病性禽流感免疫的出口家禽,有关企业报省级兽医主管部门批准后,可以不实施免疫。强制免疫的疫苗为:经国家批准使用的“重组禽流感病毒(H5+H7)二价灭活疫苗(H5N1 Re-8 株 +H7N9 H7-Re1 株)”(简称“H5+H7 二价灭活疫苗”),疫苗产品具体信息可在中国兽药信息网“国家兽药基础信息查询”平台“兽药产品批准文号数据”中查询。
从 2017 年秋季开始,全国家禽全面开展了“H5+H7 二价灭活疫苗”的免疫,在 2017 年秋防和 2018 年春防取得了明显的防控成效。所以,加强生物安全管理,做好疫苗的免疫,高致病性禽流感是可防可控的。
应用优质的禽流感疫苗,是防控禽流感的关键措施之一,优质禽流感疫苗应包含这些要素:制苗毒株的针对性强,抗原含量足和效价高、免后抗体水平高及免疫副反应轻等。禽流感灭活疫苗的制备过程,包括:毒种的选育、半成品病毒液的制备、病毒液的灭活和疫苗的乳化等多个环节,按照 GMP 的管理要求,每一个生产环节完成,须检验合格后才可进入下一个生产环节,通过生产全过程每个环节的质量把关,确保最终生产出来的疫苗全面符合质量标准的要求。
“永顺生物”是我国最早获批的高致病性禽流感疫苗定点生产企业之一,多年来,通过不断完善质量管理制度,有效落实 GMP 管理措施,使得禽流感灭活疫苗的质量水平在全国名列前茅。现就禽流感灭活疫苗制备过程的质量控制简述如下。
1、毒种选育与半成品制备的质量控制
1.1 毒种的筛选与繁育
“H5+H7 二价灭活疫苗”制苗用的基础毒种是哈尔滨兽医研究所(国家禽流感参考实验室)利用反向遗传操作技术构建而成的,用于构建制苗毒种的基因供体毒株是当前最具代表性的 H5 和 H7 亚型禽流感病毒株,其中 H5N1 Re-8 株针对的是 H5 亚型禽流感主要流行的基因型clade 2.3.4.4 分支;H7-Re1 株针对的是 H7N9 亚型禽流感。
由基础毒种制备生产毒种,质量控制的关键点是: (1)选用有质量保证的优质 SPF 鸡胚进行毒种复壮和繁育,确保所制备的生产毒种纯净和高效价。(2)选择最适合的毒种稀释倍数稀释毒种进行接种。(3)接种后的鸡胚控制在 36~37℃进行后孵化。(4)确保接种后的鸡胚有足够的孵育时间。(5)准确测定病毒液的 HA 效价,从中选择 HA 效价高的病毒液留作毒种。通过对这些质量关键点进行严格的把控,制备的 H5N1 Re-8株和 H7N9 H7-Re1 株生产毒种可以达到 HA 效价≥1∶512,每 0.1mL病毒含量≥108.0 EID50,为生产优质疫苗打下坚实基础。
1.2 半成品病毒液的制备
制备了生产毒种,下一个生产工序是制备大批量的半成品病毒液,这个环节质量控制的关键点是: (1)选用 H5 和H7 亚型禽流感非免疫蛋鸡所生产的新鲜、洁净、均一和无畸形的受精鸡蛋,孵化至 10~11日龄的鸡胚,用这种易感而有活力的鸡胚进行病毒培养,制备高效价的病毒液。(2)用合适的稀释倍数稀释毒种进行接种,有效提高毒种的复制效力。(3)在接种过程严格执行无菌操作程序,避免细菌污染致死鸡胚而不能进行正常的病毒培养。(4)大批量生产过程中,后孵化的鸡胚密度大,要控制后孵化的温度在 36~37℃之间。(5)确保接种后的鸡胚有足够的孵育时间。(6)在收获病毒液前,鸡胚应在 2~8℃完全冻透,血管和蛋黄收缩良好,使所收获的病毒液杂质少、收量多。通过在这些关键点实施有效的质量控制,制备的病毒液杂质少、效价高,为生产优质疫苗提供基本保障。这个环节做得好与差,所制备的半成品病病毒液有明显的质量差异,具体数据见表 1。
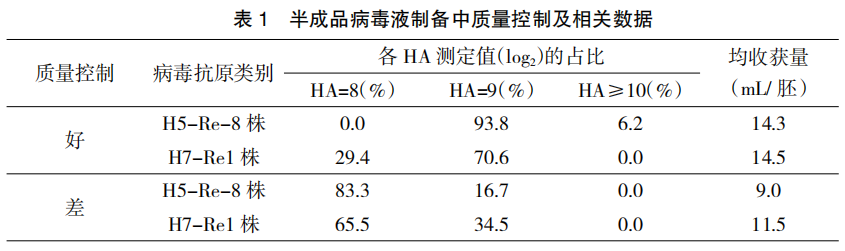
以上介绍了禽流感灭活疫苗制备过程中毒种的选育、半成品病毒液的制备两个生产环节的质量控制,以下为检验篇。
2、原材料生产工序与产品检验
禽流感灭活疫苗的制备过程包括毒种的选育、半成品病毒液的制备、病毒的灭活、疫苗的乳化和分装等多个环节,按兽药 GMP 的管理原则,疫苗质量是通过生产过程的质量控制来实现的,这一质量管理的指导思想是全员参与质量管理,严格执行生产操作技术规范,从原材料使用到生产每道工序每个环节都严格进行质量把关,确保疫苗的生产严格按经过验证的工艺进行,从而使最终生产出来的疫苗全面达到质量标准的要求。
在实施全面质量管理的过程中,快速而准确的检验是关键的技术支撑。对疫苗制备过程的质量控制,须严格按各生产工序的质量标准进行检验,准确地给出检验结果,才能杜绝不合格的半成品进入下一道生产工序;对疫苗成品的检验,也必须按疫苗制造与检验规程的质量标准全面进行检验,保证检验结果的真实可靠,才能确保不合格的产品不出厂。现就“H5+H7二价灭活疫苗”质量控制过程中的检验要点简述如下。
2.1 主要原材料的检验
2.1.1 非免疫受精鸡蛋的检验
每一批受精鸡蛋经检验合格才投入使用,使孵化至 10~11 日龄的鸡胚为健康易感鸡胚,从而使制备的半成品病毒液效价高、纯净性好,是保证疫苗品质优良的基础。按非免疫受精鸡蛋的质量标准,须快速准确进行检验的项目包括:(1)鸡蛋的外观洁净、均一、无畸形和无破损; (2)蛋的重量适中,在 50~70g 之间;(3)萃取蛋黄液用 H5 和 H7 亚型禽流感抗原检测 HI抗体,HI 抗体效价均应<1:2,确保鸡蛋产自 H5和 H7 亚型禽流感疫苗非免疫蛋鸡群。
2.1.2 注射用白油的检验
“H5+H7 二价灭活疫苗”为油包水型油乳剂疫苗,选用优质的注射用白油才能保证疫苗的稳定性,提高疫苗的免疫效力和减轻疫苗的不良反应。按《中国兽药典》(2015 版)的质量标准,注射用白油的主要检验项目有:(1)性状为无色透明、无臭、无味的油状液体; (2)相对密度为 0.818~0.880;(3)稠环芳烃:其最大吸光度不得超过 0.10;(4)重金属:含重金属应不超过1×10-5;(5)铅:含铅应不超过 1×10-6;(6)砷:含砷应不超过 1×10-6 。
2.2 疫苗制备过程的半成品检验
2.2.1 生产用毒种的检验
毒种的纯净和高效价是生产高质量半成品病毒液的根本保证,对每批生产用毒种必须严格地进行系统的检验,符合要求才可用于生产。对生产用毒种的检验包括:(1)选用健康的 10日龄 SPF 鸡胚测定毒种的病毒含量,准确配制1%的鸡红细胞悬液测定毒种的 HA 效价,保证检验的准确性,确保毒种的病毒含量和 HA 效价符合质量标准;(2)按《中国兽药典》(2015版)的操作规范和标准对毒种进行纯净性检验,确保毒种无细菌、霉菌、支原体及外源病毒污染;(3)用微量法 HI 试验对毒种进行特异性检验,H5N1 Re-8 株毒种应只对禽流感病毒 H5亚型单特异性 抗血清为阳性反应 ,H7N9H7-Re1 株毒种应只对禽流感病毒 H7 亚型单特异性抗血清为阳性反应。
2.2.2 半成品病毒液的效价检验
准确配制 1%的鸡红细胞悬液用微量法HA 试验,对半成品病毒液抽样进行 HA 效价检验,符合质量标准才能进入下一生产环节。
2.2.3 病毒液灭活后的无菌检验
对灭活后的 H5N1 Re-8 株 和 H7N9H7-Re1 株病毒液分别抽样,按《中国兽药典》(2015 版)的操作规范和标准进行无菌检验,应无菌生长才可用于配制疫苗。
2.2.4 病毒液灭活后的灭活检验
对灭活后的 H5N1 Re-8 株 和 H7N9H7-Re1 株病毒液分别抽样,用健康的 10 日龄SPF 鸡胚,按疫苗制造与检验规程的操作规范和标准进行灭活检验,经检验确认病毒已灭活完全才能用于配制疫苗。
2.3 成品的检验
分装后的疫苗成品必须按规定留样进行全面的质量检验,根据疫苗制造与检验规程的要求,成品检验的项目包括:(1)外观为乳白色均匀乳剂;(2)剂型为油包水型;(3)疫苗的稳定性检验:取 10mL 疫苗以 3 000r/min 离心 15min,管底析出的水相应不超过 0.5mL;(4)装量检查、无菌检验、黏度及甲醛残留量测定,均要符合《中国兽药典》(2015 版)的规定;(5)在负压隔离器,按疫苗制造与检验规程的操作规范和标准进行安全检验、效力检验,均须符合规定。
疫苗、药品是用于防病治病的特殊产品,国际上对疫苗、药品质量管理的理念有一个不断变化的过程,从“质量是检验出来的”到“质量是生产出来的”,进而又到“质量是通过良好的设计而生产出来的”等。然而,不管如何变化,所有质量管理的有效实施都离不开严谨而精确的检验作为技术支撑。
作者:李永红,肖永珍(广东永顺生物制药股份有限公司,广州510640)
责任编辑:李斐







